嵌合抗原受體T細胞(CAR-T)療法作為腫瘤免疫治療領域的一項革命性突破,已從實驗室研究迅速走向臨床應用,為血液系統惡性腫瘤患者帶來了前所未有的治愈希望。這一開創性療法的發展歷程,既充滿了激動人心的機遇,也面臨著嚴峻的科學與臨床挑戰,其未來的成熟與普及,高度依賴于持續深入的工程、技術研究與試驗發展。
一、 歷史性機遇:從概念驗證到臨床轉化
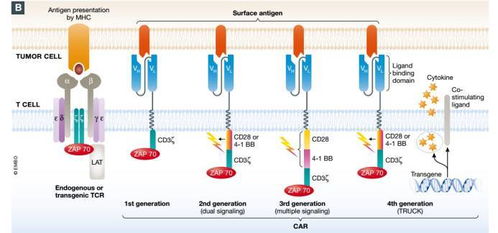
CAR-T療法的核心機遇在于其能夠“重新編程”患者自身的免疫細胞,使其具備精準識別并高效清除腫瘤細胞的能力。自2017年首款CAR-T產品獲美國FDA批準以來,該療法已在復發/難治性B細胞淋巴瘤、白血病等疾病中展現出卓越的療效,部分患者甚至達到長期完全緩解,實現了從“絕癥”到“可治”的范式轉變。這不僅是腫瘤治療領域的里程碑,更開辟了個體化、活細胞藥物這一全新賽道,吸引了全球學術界和產業界的巨額投入與高度關注。
二、 當前面臨的臨床挑戰
盡管前景廣闊,CAR-T療法的臨床推廣仍面臨多重瓶頸:
- 安全性風險:細胞因子釋放綜合征(CRS)和免疫效應細胞相關神經毒性綜合征(ICANS)是常見且可能危及生命的嚴重不良反應,其發生機制與預測模型仍需深入研究。
- 實體瘤療效有限:相較于血液瘤,CAR-T在實體瘤治療中效果不佳,面臨腫瘤微環境抑制、靶抗原異質性、細胞浸潤困難等“壁壘”。
- 可及性與成本:自體CAR-T療法制備流程復雜、周期長、成本極其高昂,限制了其惠及更廣泛的患者群體。
- 耐藥與復發:部分患者會出現靶抗原丟失或T細胞功能耗竭,導致治療無效或疾病復發。
三、 工程與技術創新:破局的關鍵路徑
應對上述挑戰,未來的發展重心必須置于跨學科的工程與技術研究與試驗發展(R&D)上:
- 新一代CAR結構工程:研發包含共刺激域、安全開關、邏輯門控(如“與”門)的智能型CAR,以提升特異性、持久性并降低脫靶毒性。
- 通用型(“現貨型”)CAR-T技術:通過基因編輯技術(如CRISPR/Cas9)敲除宿主T細胞的排斥相關基因,開發源自健康供體的同種異體CAR-T產品,旨在實現標準化、規模化生產,降低成本與等待時間。
- 實體瘤微環境改造策略:結合CAR-T與免疫調節劑、溶瘤病毒或靶向腫瘤基質的療法,改造免疫抑制性微環境,增強T細胞浸潤與功能。
- 先進制造與自動化工藝:開發封閉式、自動化的細胞生產系統,優化載體轉導效率,建立嚴格的質量控制體系,是確保產品一致性、安全性與可擴展性的工程基礎。
- 新型遞送與基因編輯技術:探索非病毒載體(如轉座子/轉座酶系統)進行基因遞送,以及更精準、高效的體內基因編輯技術,為實現體內直接制備CAR-T細胞提供可能。
四、 展望未來
CAR-T療法的故事遠未結束,它正從一個針對特定血液瘤的“特效藥”,向著一個可編程、可調控的通用型細胞治療平臺演進。這一進程的成功,有賴于生命科學家、臨床醫生、生物工程師、數據科學家和監管機構的緊密協作。通過持續的基礎研究厘清作用機制,通過巧妙的工程學設計優化產品性能,并通過嚴謹的臨床試驗驗證安全有效,我們才能逐步攻克現有難題,解鎖CAR-T療法在更廣泛疾病領域(包括自身免疫性疾病、慢性感染等)的應用潛力,最終將這種“活的藥物”轉化為惠及全球患者的常規治療選擇。機遇與挑戰并存,正是技術創新驅動醫學進步的生動寫照。